 干货│基因编辑探秘系列之在动植物育种领域的应用
干货│基因编辑探秘系列之在动植物育种领域的应用
11522
2024-08-29
2024年5月29日,美国农业部宣布苏州齐禾生科生物科技有限公司研发的基因编辑高油酸大豆P16获得监管豁免。这标志着中国在美国市场成功获得首个基因编辑产品的监管豁免,展示了中国在生物技术领域的竞争力和基因编辑技术在农业育种方面的巨大潜力。齐禾生科通过对大豆内源脂肪酸脱氢酶基因进行精准编辑,成功培育出高油酸大豆P16。这一突破性成果不仅优化了大豆的油脂组成,使大豆种子中的油酸含量提升至80%以上,还可能对提升其商业价值和市场竞争力产生积极影响。
CRISPR基因编辑技术,作为继野生驯化、杂交和转基因之后的第四代育种技术,标志着4.0育种时代的来临。这项技术在改良重要经济物种性状方面展现出了巨大的潜力,本文将从植物和动物育种两个方向为大家详细介绍CRISPR技术的应用。
植物基因编辑育种
在植物育种领域,农作物作为基因编辑技术的明星对象,已经取得了令人瞩目的成就。诸如糯玉米、高油酸大豆、抗褐变马铃薯、高GABA番茄、抗褐变蘑菇、抗除草剂水稻和抗除草剂玉米等基因编辑产品,在美国、日本等国家的市场上熠熠生辉,充分展现了基因编辑技术的巨大潜力。
玉米,这种重要的粮食和饲料作物,其关键性状的优化和育种技术的发展具有深远的意义。在这方面,CRISPR技术如同一把神奇的钥匙,已广泛应用于玉米的品质改良。它涉及多个方面,包括提升产量(例如通过减小叶夹角以增加种植密度,进而提高行和籽粒产量)、改善食用品质(如培育出糯玉米和甜玉米品种)、增强抗逆性(例如提升耐旱能力和抗除草剂能力),以及调控开花时间(在长日照条件下促使更早开花)等。接下来,小编将以玉米为例,为大家详细介绍基于CRISPR技术的植物育种流程。
植物基因编辑的过程一般可分为六个步骤:
设计阶段
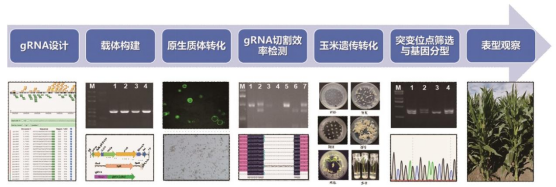
图1. 基于CRISPR/Cas9系统的玉米基因组编辑技术流程[2]
与在植物育种领域的广泛应用相呼应,基因编辑技术在动物育种领域同样展现出了其广泛的适用性和潜力。
动物基因编辑育种
基因编辑技术在动物育种领域的应用范围极为广泛。在改良生产性能方面,通过编辑动物基因组,改良畜禽经济性状,比如加快生长速度,提高饲料利用率等;在改善肉质方面,基因编辑方法既可以降低动物脂肪量,还能够调整其肌肉组织的构成,以生产更符合市场和消费者需求的肉类产品;在增强家畜抗病能力方面,通过基因编辑开发出具备特定疾病抗性的新品种,能显著提高动物种群的基因适应性,减少养殖业中抗生素的使用量。这一举措不仅有助于保障人类健康,同时也是推动环境可持续发展战略的关键因素[3]。下面,以基因编辑猪为例,我们将具体阐释动物基因编辑的操作流程,揭示这项先进技术如何在现代畜牧业中发挥作用。
动物基因编辑的过程一般可分为六个步骤:
设计阶段
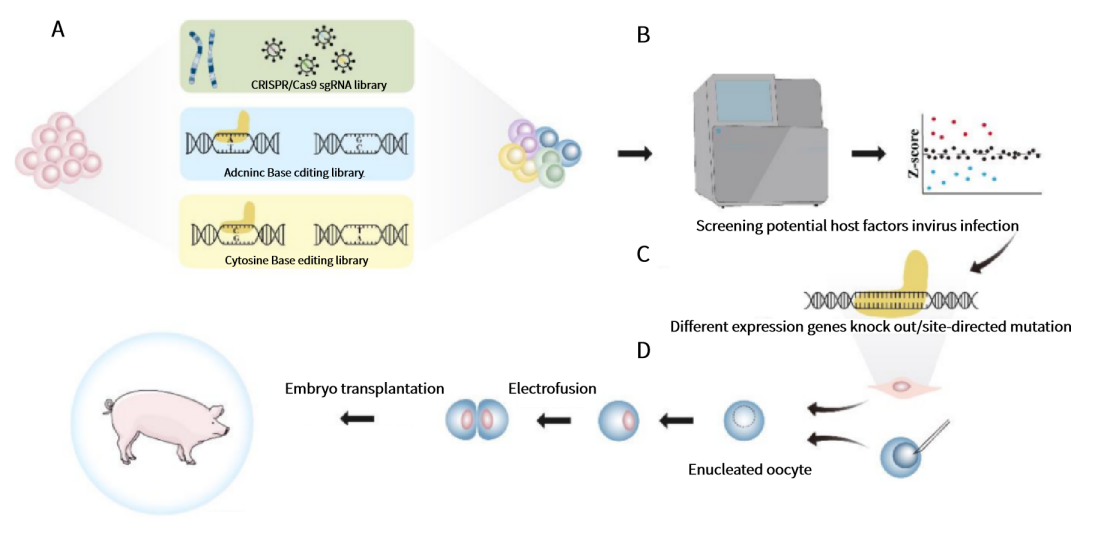
图2. 基于CRISPR/Cas9系统的基因编辑猪技术流程[4]
基因组编辑技术的迅猛进展在基因功能探究与作物特性优化等领域已实现重大突破。随着CRISPR/Cas系统的持续进化与精进,基于基因组编辑的前沿育种技术将进一步与高通量表型分析、基因组选择、快速育种等尖端技术深度整合,为农业及畜牧业的创新发展注入强大动力。
产品推荐
|
产品应用 |
产品定位 |
产品名称 |
产品货号 |
|
通用型 |
带NLS的SpCas9 |
14701ES |
|
|
荧光观察/流式分选 |
带EGFP荧光标签的SpCas9 |
11364ES |
|
|
基因调控 |
无剪切酶活性的Cas9 |
11351ES |
|
|
小分子量递送 |
Cas12a |
14702ES |
|
|
Cas12b |
14808ES |
||
|
sgRNA制备 |
sgRNA合成 |
11355ES |
|
|
sgRNA纯化 |
12602ES |
参考文献:
[1] Gao C. Genome engineering for crop improvement and future agriculture. Cell. 2021 Mar 18;184(6):1621-1635.
[2] 杨梦冰, 江易林, 祝蕾, 安学丽, 万向元. CRISPR/Cas植物基因组编辑技术及其在玉米中的应用. 中国生物工程杂志, 2021, 41(12): 4-12.
[3] 张格阳, 张子敬, 翟亚莹, 吕世杰, 朱肖亭, 朱进华, 李峥, 于翔, 王红利, 施巧婷, 闫祥洲, 王二耀. 基因编辑技术在我国畜牧业的研究进展[J]. 中国畜禽种业, 2022, 18(10): 45-48.
[4] Randall, S, Prathe, et al. Generation of a Commercial-Scale Founder Population of Porcine Reproductive and Respiratory Syndrome Virus Resistant Pigs Using CRISPR-Cas [J]. Scientific Reports, 2017. DOI:10.1038/s41598-017-13794-2.





