干货│基因编辑探秘系列之在体外诊断领域的应用
干货│基因编辑探秘系列之在体外诊断领域的应用
11178
2024-08-08
近年来,随着诊疗体系从传统的以医院为中心变为去中心化,检测场景从医院检测变成社区或家用检测,开发规模化、自动化、快速化的检测技术成为趋势。科学界发现CRISPR/Cas系统除在基因编辑领域的应用以外,在POCT检测工具开发方面同样具有独特的优势,将现有技术结合CRISPR/Cas系统,有望开发速度更快、灵敏度更高、成本更低、检测特异性更好、操作更便利的POCT检测工具。目前,基于不同的Cas蛋白,研究者们已经成功开发出多种创新的检测方法,为未来体外诊断技术的发展奠定了坚实的基础。
|
Cas蛋白 |
分类 |
向导RNA |
反式切割酶活性 |
蛋白大小 |
靶标分子 |
应用技术平台 |
|
Cas9 |
II型 |
gNDA (tracRNA+crRNA) |
无 |
~1400aa |
dsDNA |
NASBACC |
|
Cas12a |
V型 |
crRNA |
有(ssDNA) |
100~1300aa |
dsDNA、ssDNA |
DETECTR、HOLMES |
|
Cas12b |
V型 |
gNDA (tracRNA + crRNA) |
有(ssDNA) |
700~1000aa |
dsDNA、ssDNA |
C Detection 、HOLMES V2 |
|
Cas13a |
VI型 |
crRNA |
有(ssRNA) |
700~1000aa |
ssRNA |
SHERLOCK |
|
Cas14a (Cas12f) |
V型 |
gNDA (tracRNA+crRNA) |
有(ssDNA) |
400-700aa |
ssDNA、dsDNA |
DETECTR-Cas14 |
图1.不同Cas蛋白特点及应用[1]
基于Cas9的检测系统
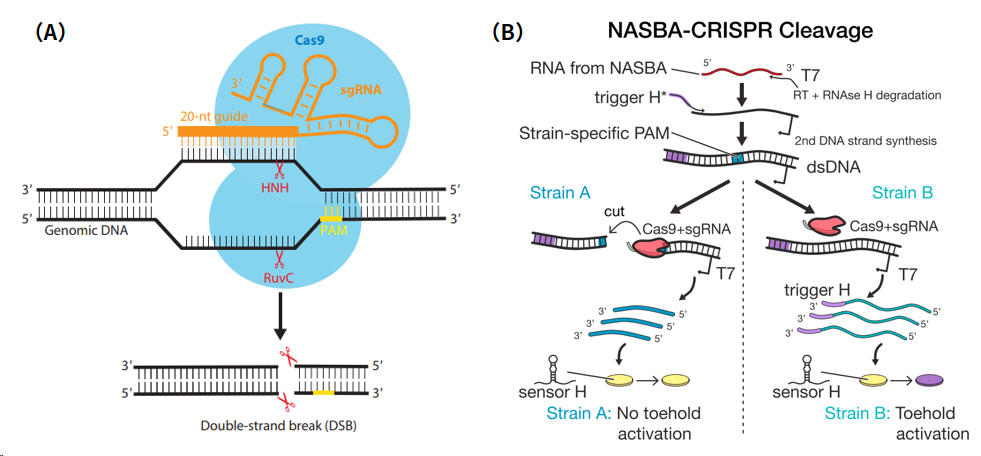
Cas9属于II型系统,有两个内切酶功能域RuvC和HNH,在sgRNA的引导下,Cas9通过识别靶标DNA上的PAM序列,特异性地与靶标DNA结合,并切割靶标DNA,其原理如图2(A)所示。
基于Cas12的检测系统
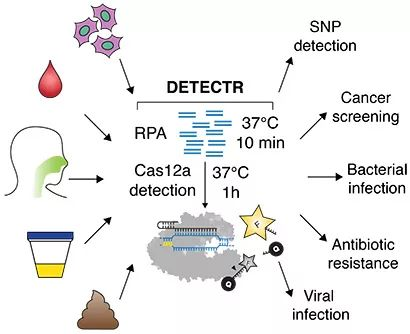
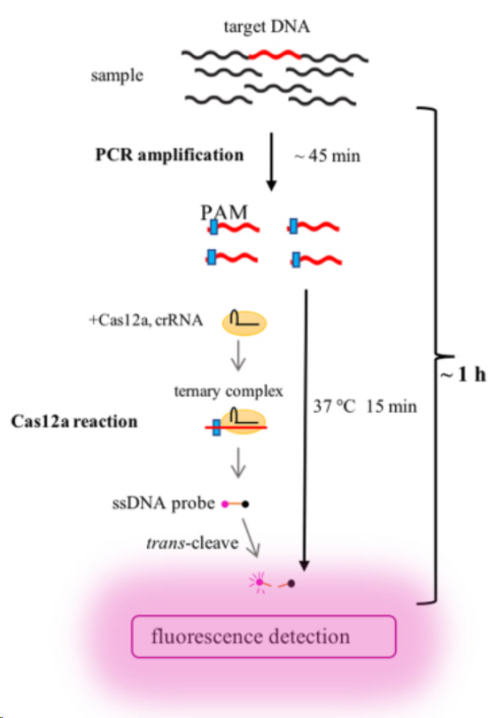
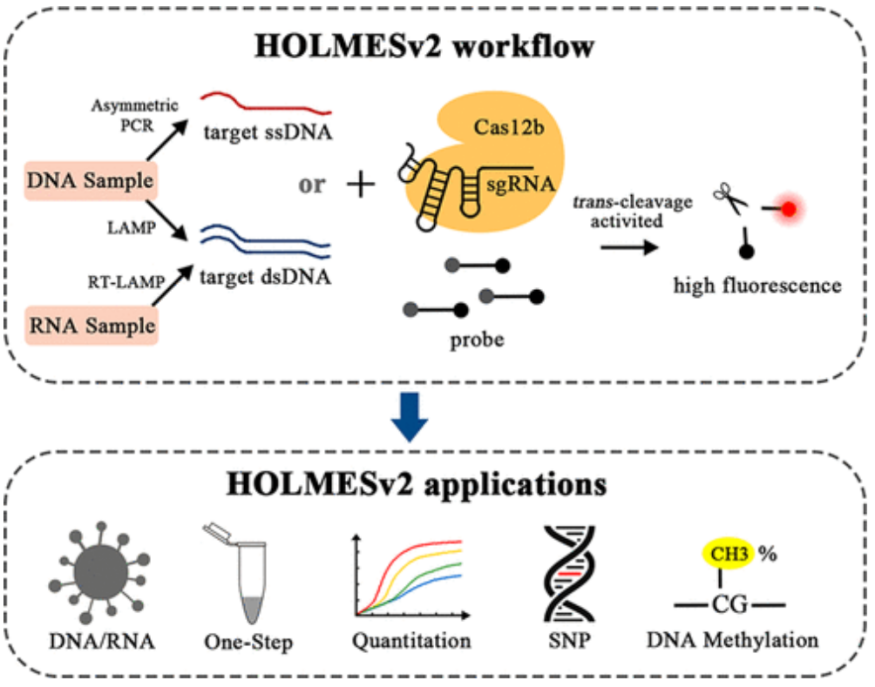
与Cas9不同,Cas12除了能以PAM依赖的方式识别和切割dsDNA,还能够不依赖PAM序列特异性识别并切割ssDNA(单链DNA)。此外,Cas12除靶标DNA切割活性外,在Cas12、sgRNA和靶标DNA形成三元复合物后,能激发其反式切割活性,将体系中任意ssDNA序列切碎。利用其反式切割活性,研究者们基于Cas12a和Cas12b构建了多种新型核酸诊断技术,大大提高了病原体或疾病诊断的灵敏度和准确性。
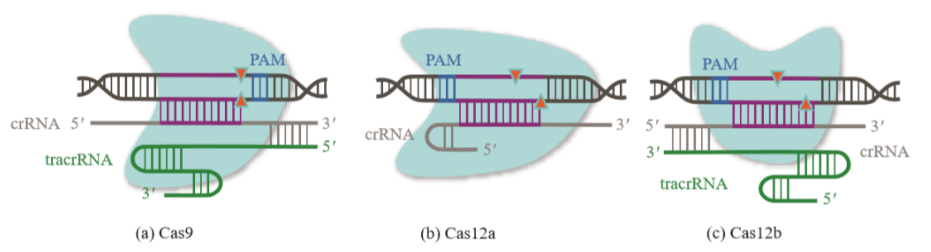
图3.不同Cas蛋白作用原理[4]
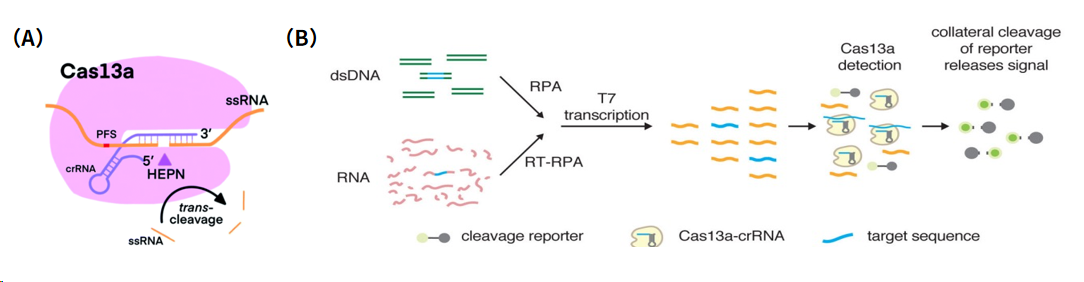
基于Cas13的检测系统
Cas13属于VI型系统,具有靶向切割目标RNA的能力。Cas13含有两个高等真核生物和原核生物核苷酸(HEPN)结合域,Cas13仅凭单个crRNA的引导便可与靶标RNA进行碱基互补配对,并特异性地对靶标RNA进行顺式剪切。此外,与Cas12类似,Cas13也具有反式切割活性,在识别到特定的RNA序列后,将体系中任意ssDNA序列切碎,其原理见图6(A)。这一特性使得Cas13成为检测RNA的理想选择,特别是在病毒性疾病的快速诊断中显示出巨大的应用潜力。
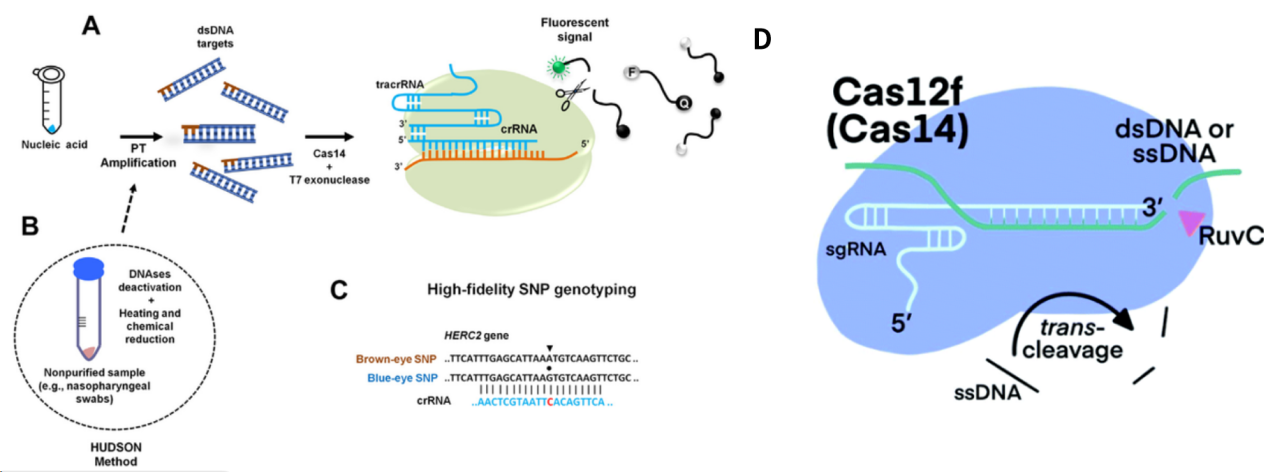
基于Cas14的检测系统
Cas14属于V型系统,是一个非常紧凑的RNA引导核酸酶家族(400到700个aa),其大小仅为Cas9和Cas12的一半。Cas14具备不依赖PAM切割和反式切割ssDNA能力,同时可在PAM的引导下切割dsDNA。与Cas12不同,Cas14对靶标与crRNA之间的核苷酸碱基错配的耐受性较低,导致可靶向范围窄,能够用于高精度的核酸检测,如单核苷酸多态性基因分型。
CRISPR/Cas系统作为基因编辑和体外诊断技术的基石,不同的Cas蛋白在应用中展现出各自独特的功能和优势,这些特性使得各个Cas蛋白在体外诊断检测系统中展现出了巨大的潜力和广阔的应用前景。随着技术的不断进步和创新,CRISPR/Cas技术将在未来的医疗健康领域发挥更加重要的作用。
相关产品推荐
|
产品定位 |
产品名称 |
产品货号 |
|
Cas系列 |
Cas9 Nuclease |
|
|
ArCas12a Nuclease |
||
|
AapCas12b Nuclease |
||
|
RT-LAMP系列 |
Hieff® Bst Plus DNA Polymerase (40 U/μL) |
|
|
Hifair® III Reverse Transcriptase |
||
|
RPA系列 |
Bsu DNA polymerase (Large fragment, 5 U/μL) |
|
|
T4 UvsX Recombinase (2 μg/μL) |
||
|
T4 UvsY protein (2 μg/μL) |
||
|
T4 gene 32 protein (gp 32) T4噬菌体基因32编码蛋白 |
||
|
Creatine Kinase (2 μg/μL) 肌酸激酶 |
||
|
Exonuclease III (100 U/μL) |
参考文献
[1] 孙雯君,黄行许,王鑫杰.基于CRISPR的快速灵敏便捷分子检测[J].生物工程学报, 2023, 39(1):14.
[2] Jiang, F, Doudna, J. A. (2017). CRISPR-Cas9 Structures and Mechanisms. Annual review of biophysics, 46, 505–529.
[3] Pardee K, Green AA, Takahashi MK, et al. Rapid, Low-Cost Detection of Zika Virus Using Programmable Biomolecular Components. Cell. 2016 May 19;165(5):1255-1266.
[4] Li L, Li S, Wang J. CRISPR-Cas12b-assisted nucleic acid detection platform[J].Cold Spring Harbor Laboratory, 2018(10).DOI:10.1101/362889.
[5] Chen JS, Ma E, Harrington LB, et al. CRISPR-Cas12a target binding unleashes indiscriminate single-stranded DNase activity [published correction appears in Science. 2021 Feb 19;371(6531):]. Science. 2018;360(6387):436-439. doi:10.1126/science.aar6245.
[6] Li S Y, Cheng Q X, Wang J M, et al. CRISPR-Cas12a-assisted nucleic acid detection[J]. Cell discovery, 2018, 4(1): 20.
[7] Li L, Li S, Wu N, et al. HOLMESv2: A CRISPR-Cas12b-Assisted Platform for Nucleic Acid Detection and DNA Methylation Quantitation. ACS Synth Biol. 2019;8(10):2228-2237. doi:10.1021/acssynbio.9b00209.
[8] Myhrvold C, Freije CA, Gootenberg JS, et al. Field-deployable viral diagnostics using CRISPR-Cas13. Science. 2018 Apr 27;360(6387):444-448.
[9] Harrington LB, Burstein D, Chen JS, et al. Programmed DNA destruction by miniature CRISPR-Cas14 enzymes. Science. 2018;362(6416):839-842. doi:10.1126/science.aav4294.
<上下滑动查看更多>