 翌圣ELISA产品助力肿瘤免疫治疗新突破:导电纳米酶诱导原位肿瘤疫苗”
翌圣ELISA产品助力肿瘤免疫治疗新突破:导电纳米酶诱导原位肿瘤疫苗”
249
2026-04-24
近年来,免疫疗法已成为癌症治疗领域的革命性力量。然而,如何在激活强效抗肿瘤免疫的同时,避免对正常组织的损伤,始终是该领域面临的重大挑战。近日,来自重庆医科大学附属第二医院超声科的赵浩团队在这一难题上取得了突破性进展。
该研究成果发表于国际顶级期刊 《Signal Transduction and Targeted Therapy》 (IF=52.7),题为 “Conductive coordination nanozyme prodrugs precisely trigger pyroptosis, cuproptosis and ferroptosis for in situ cancer vaccination” 。
研究团队创新性地设计了一种导电配位纳米酶前药 Cu-DHN,通过肿瘤微环境特异性激活,同步触发焦亡 + 铜死亡 + 铁死亡,实现原位肿瘤疫苗与强效抗肿瘤免疫,安全性与疗效双优,为肿瘤免疫治疗开辟了新路径。

值得关注的是,该研究在关键炎症因子检测环节,使用了翌圣生物(Yeasen)的Mouse IL-1β ELISA Kit(货号:98024ES),为验证纳米酶诱导的焦亡效应提供了可靠数据支撑。
焦亡(Pyroptosis)是一种炎性程序性细胞死亡方式。它能快速将肿瘤细胞内的“危险信号”和肿瘤抗原释放出来,如同一场“就地取材”的疫苗制备过程,能有效激活全身抗肿瘤免疫。然而,焦亡疗法面临两大“拦路虎”:
肿瘤特异性差:多数肿瘤中焦亡执行蛋白GSDM(Gasdermin)表达水平低,如同“有枪无弹”,导致焦亡难以启动。
系统毒性高:直接使用焦亡激活剂会无差别攻击正常组织,引发严重副作用。
如何构建一个能在肿瘤部位特异性激活、并克服GSDM低表达障碍的“智能”系统,是解决上述问题的关键。
整个实验设计中,为了严谨验证Cu-DHN能否真正诱导焦亡,研究团队进行了一系列分子生物学实验。其中,检测焦亡的关键下游炎性因子——白细胞介素-1β (IL-1β) 的分泌水平是重中之重,IL-1β的成熟和释放是焦亡通路激活的“金标准”之一。如下图所示,研究团队检测了不同处理后,4T1小鼠乳腺癌细胞上清中的IL-1β含量。

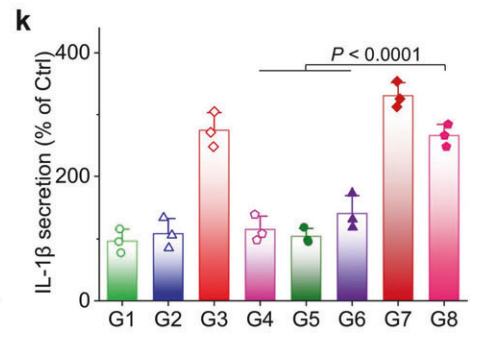
Fig 4k. IL-1β secretion from 4T1 cells after co-incubation with Cu–DHN for 18 h (n = 3).
与PBS对照组相比,经Cu-DHN处理后的细胞,其IL-1β的分泌量出现了极显著的升高。这一结果直接证明了:Cu-DHN成功激活了NLRP3炎症小体。激活的caspase-1有效切割了GSDMD蛋白。焦亡孔洞的形成导致了IL-1β等炎性因子的大量释放。
这些数据为Cu-DHN诱导高效焦亡提供了直接、可靠的证据。翌圣ELISA试剂盒以其高灵敏度、高特异性和稳定的批间差,帮助研究者获得了清晰、可信的关键数据,有力支撑了文章的结论。
高精密度:酶标板内/板间精密度高,批次间差异小;
高灵敏性:灵敏度可达pg级别,标曲稳定,精准定量低丰度样本;
定量准确:检测范围广,回收率高,真实反映样本中的含量;
多样本适用:已验证过血清、血浆、细胞培养上清等常见样本类型;
|
产品名称 |
规格 |
产品货号 |
|
Human IFN-γ ELISA Kit |
96T |
|
|
Human TNF-α ELISA Kit |
96T |
|
|
Human IL-15 ELISA Kit |
96T |
|
|
Human PD-L1 ELISA Kit |
96T |
|
|
Human IL-1β ELISA Kit |
96T |
|
|
Human IL-2 ELISA Kit |
96T |
|
|
Human IL-10 ELISA Kit |
96T |





