Hieff NGS® OnePot Flash DNA Library Prep Kit/ 低背景病原快速酶切DNA建库试剂盒
产品介绍
Hieff NGS® OnePot Flash DNA Library Prep Kit 是快速版酶切法建库试剂盒,本品采用高质量的片段化酶,将片段化模块与末端修复/加A模块合二为一,简化了操作流程,极大的降低了建库的时间和成本。适用于100 pg-500 ng常规动植物基因组、微生物基因组等样本,在单管内快速实现DNA的片段化、末端修复和A尾添加反应。本试剂盒需自行搭配接头和引物,可同时兼容Illumina®和MGI®高通量测序平台。
产品特色
省时:2 h内极速建库,单管酶切、 末修和加A 10 min
省力:单管酶促反应,酶切
省样本:兼容低至100 pg样本建库
背景菌干净,宿主核酸残留低
应用案例
1、快速建库文库产出
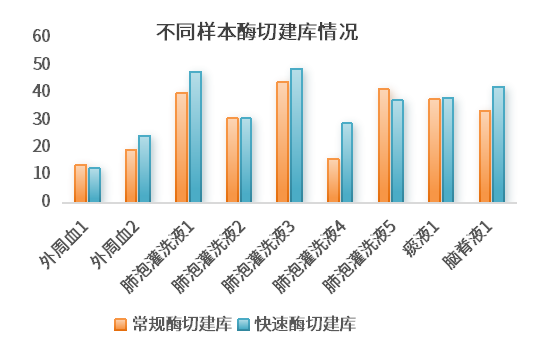
2、多样本兼容性(gDNA&cfDNA&cDNA&PCR产物)
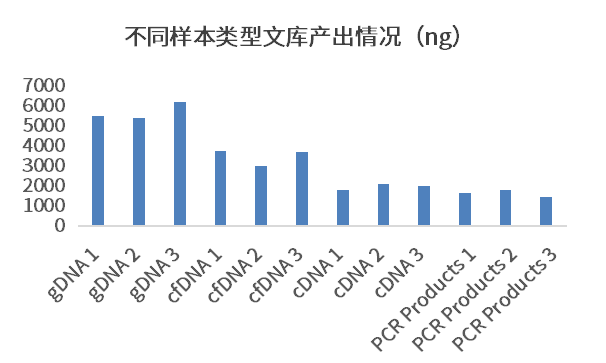
3、低丰度病原体检出情况
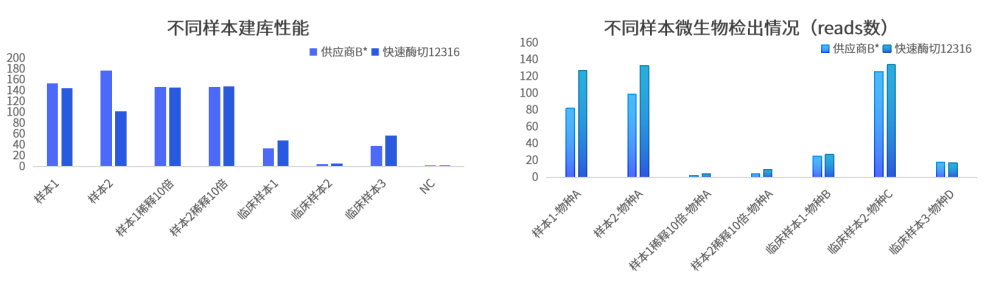
存储条件
-25~-15℃保存,有效期1年。
COA
已发表文献
相关产品
推荐应用
联系我们





