 脂多糖(LPS)炎症模型的建立
脂多糖(LPS)炎症模型的建立
20161
2024-08-19
脂多糖简介
脂多糖(Lipopolysaccharide, LPS)是革兰氏阴性细菌外膜的主要成分之一,由类脂A、核心多糖和O-抗原三部分组成,其中O-抗原决定了LPS的血清型,具有重要的生物学功能和作用机制。LPS在细菌正常生活状态时不释放,但在细菌菌体死亡破裂或人工方法裂解后会释放出来,作为非特异性免疫原,与宿主效应细胞相互作用,引起机体发热、弥散性血管内凝血、多器官机能衰竭等。
脂多糖作用机制
LPS的毒性主要通过与宿主细胞的TLR4受体结合来发挥,这一过程涉及内毒素结合蛋白、CD14分子和MD-2分子的协同作用。LPS与TLR4结合后,激活细胞内信号传导途径,包括髓样分化因子88(MyD88)、IL-1受体相关激酶(IRAK)等,最终激活转录因子NF-κB,导致炎症因子的产生和释放。
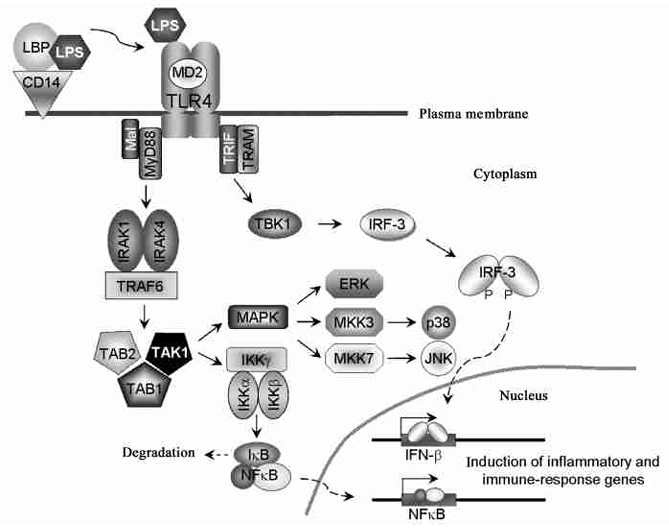
图1.脂多糖信号通路的示意图[1]
脂多糖应用
LPS在生物医学研究中具有重要应用,例如在研究神经炎症模型中,LPS常被用作诱导炎症反应的试剂,模拟由革兰氏阴性菌感染引起的炎症过程。翌圣生物提供来源于大肠杆菌的2种脂多糖,产品相关介绍如下:
|
货号 |
60747ES |
60748ES |
|
名称 |
||
|
血清型 |
O55:B5 |
O111:B4 |
|
主要应用 |
体外细胞活化; 用于内毒素LAL检测; 作为疫苗佐剂增强免疫原性; 用于感染和炎症反应机制的研究; 可能更适合于体外细胞活化和炎症研究。 |
刺激体内猪肝脏组织和体外仔猪回肠组织的炎症反应; 刺激体外自然杀手(NK)细胞和肝B细胞; 诱发标准兔模型中的关节炎; 可能更适合于研究B细胞激活和NOS诱导。 |
|
相同点 |
两者均可通过与宿主细胞表面的Toll样受体4(TLR4)结合来激活先天性免疫系统细胞,引发炎症反应; 两者都具有免疫原性,能够刺激免疫细胞产生炎症因子,用于模拟细菌感染过程; 两者都广泛应用于生物医学研究,特别是在炎症和免疫反应机制的研究中。 |
|
脂多糖炎症模型
LPS(脂多糖)是一种能够诱导多种炎症模型建立的内毒素,可以诱导多种炎症模型:如
1)急性肺损伤(ALI)模型:通过腹腔注射或气管给予LPS,建立急性肺损伤(ALI)模型。
2)急性胰腺炎(AP)模型:LPS与Caerulein(雨蛙素)联合使用,建立急性胰腺炎模型。
3)急性肝衰竭模型:LPS与D-(+)-氨基半乳糖联合使用,诱导急性肝衰竭模型。
4)败血症模型:通过腹腔注射LPS,建立脓毒症模型。
5)牙周炎模型:在小鼠的牙龈注射LPS诱导牙周炎模型。
6)RAW264.7细胞炎症模型:LPS可以刺激RAW264.7细胞,建立体外细胞炎症模型。
7)急性炎症小鼠模型:通过尾静脉注射或腹腔注射LPS,建立急性炎症小鼠模型。
以下面4种炎症模型为例,为您提供详细的实验模型案例,仅供参考。
4.1 LPS诱导大鼠急性肾损伤模型
4.1.1 实验方法
实验对象:2-3月龄雄性小鼠。
实验方法:禁食禁饮6小时后称量体重,按20 mg/kg体重腹腔注射新鲜配制的LPS溶液或PBS溶液,给药24h后收集实验标本。
动物处理:
1)麻醉:腹腔注射3%体积的戊巴比妥麻醉小鼠;
2)待小鼠达到麻醉效果后,快速从眼球处取血,收集在EP管中,静置约2-3h后离心(3000 rpm,10分钟),收集上清保存于-80℃冰箱备用;
3)取血后将小鼠固定于解剖板,剪开小鼠腹腔、胸腔等,将输液针从心尖部位刺入小鼠左心室,推注生理盐水,直至观察到小鼠肺、肝脏颜色变为淡红色接近于白色时停止注射生理盐水(大约30 mL);
4)停止灌注,找出双侧肾脏,摘取[2]。
4.1.2实验结果及图片
肾脏HE和PAS结果显示,LPS诱导的LPS组出现了病理损伤,近端肾小管上皮细胞脱落、肾小管结构紊乱,管腔扩张,胞浆空泡化和间质水肿。
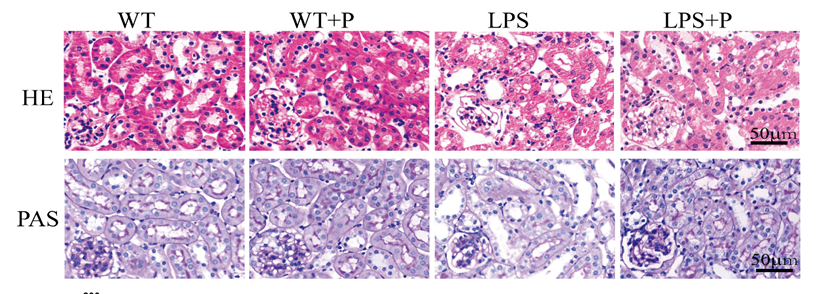
图2.不同处理方法的小鼠肾组织HE染色和PAS染色结果图[2]
4.2 LPS诱导大鼠胆色素结石模型
4.2.1实验方法
实验对象:6周龄雄性SD大鼠,体重为220 g左右。
实验方法:分别设置对照组(Control)、模型组(Model)等。模型组通过PE管注入LPS(给药剂量为5 mg/kg,浓度为1 mg/mL),分别在第3、6、9、12天给药。每次注射药物后将PE管关闭12h,然后重新打开。实验开始至第16天后,取血清、胆汁和肝脏进行后续实验。
动物处理:腹腔注射戊巴比妥钠(浓度为3 mg/mL,剂量为30 mg/kg)进行麻醉,大鼠麻醉后腹部备皮、消毒,用剪刀在腹部中央剪开一道约5 cm的创口,找到胆总管,将PE引流管插入胆总管并固定,将引流管另一端从颈部后部导出并固定,建立皮下通道。期间通过导出的引流管间断注入LPS后闭管。造模15天后,取大鼠胆汁、血清和肝脏样本。胆汁样本进行胆汁涂片,肝脏样本进行病理和分子实验[3]。
4.2.2实验结果及图片
胆汁涂片结果如图3所示,对照组大鼠的涂片较为干净,且未见结晶。而模型组大鼠胆汁明显浑浊,有黄色结晶形成,意味着造模成功。
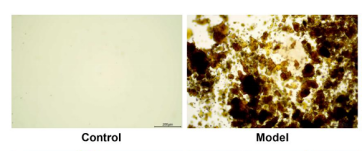
图3.各组大鼠胆汁涂片[3]
HE染色结果如图4所示,对照组大鼠肝组织结构比较正常,染色清晰,细胞表现规整,无其他明显病变。模型组大鼠肝脏大部分肝细胞发生肿胀,胞体增大,部分胞浆丢失呈网状或颗粒状,胞核皱缩深染。
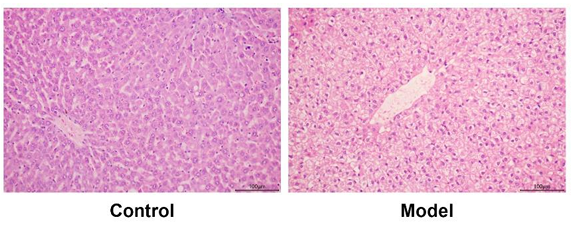
图4.各组HE染色观察肝脏组织的病理变化[3]
4.3 LPS攻毒断奶仔猪脾脏
4.3.1实验方法
实验对象:21日龄健康且体重(8.02±0.06)kg 的断奶仔猪。
实验方法:CON组和LPS组饲喂基础日粮,LPS+PEO组和LPS+CEO组分别饲喂添加500 mg/kg PEO和CEO的日粮。49日龄时,LPS组、LPS+PEO组和LPS+CEO组仔猪分别腹膜注射0.1 mg/kg体重的大肠杆菌LPS(血清型O55:B5),CON组仔猪注射等体积的无菌生理盐水,4 h后,称重后屠宰。
动物处理:剖开腹腔,采集脾脏组织,测定脾脏指数。取少量脾脏样品加入0.9%生理盐水进行稀释并利用均质器匀浆,4℃、3500 r/min离心15 min,取上清液用于免疫指标和抗氧化指标的测定[4]。
4.3.2实验结果及图片
LPS组的脾脏指数显著升高,提示脾脏可能受到了损伤。
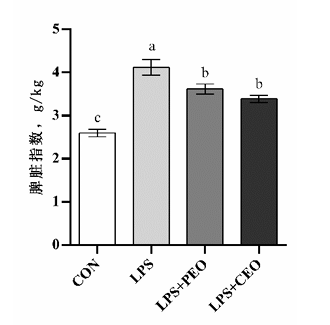
图5.各组断奶仔猪的脾脏指数[4]
4.4 巨噬细胞炎症模型构建
4.4.1实验方法
实验对象:巨噬细胞。
实验方法:当细胞生长至汇合度约90%时,弃去上清液,PBS冲洗3次。采用细胞刮刀将细胞刮下,离心5 min,使用4 mL完全培养基重悬细胞后进行计数。将细胞按每孔5x105个接种于6孔板中。将细胞随机分为空白对照组(Con组:贴壁12 h后,给予完全培养基2 mL,培养4 h)和炎症模型组(LPS组:贴壁12 h后,给予含有10 μg/mL LPS的完全培养基2 mL,培养4 h)。然后采用多种方法分析α微管蛋白乙酰转移酶1(αTAT-1)等的变化情况[5]。
4.4.2实验结果及图片
通过RT-qPCR手段检测αTAT-1等蛋白mRNA表达变化,结果显示:相比于Con组,LPS组中αTAT-1和NLRP3的mRNA表达显著增加,表明αTAT-1和NLRP3在LPS介导的巨噬细胞炎症中表达上升。
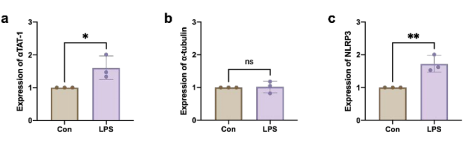
图6.巨噬细胞中αTAT-1等蛋白mRNA表达变化(a:αTAT-1;b:α-tubulin;c:NLRP3)[5]
相关产品推荐
|
产品名称 |
主要作用 |
产品货号 |
产品规格 |
|
刺激免疫应答,用于炎症相关研究 |
60747ES08/10 |
5/10 mg |
|
|
刺激免疫应答,用于炎症相关研究 |
60748ES08/10 |
5/10 mg |
|
|
联合LPS诱导胰腺炎模型 |
60321ES03 |
1 mg |
|
|
NF-κB选择性抑制剂 |
53852ES05/08 |
2/5 mg |
|
|
下调 iNOS |
57667ES08/10 |
5/10 mg |
|
|
NF-KB通路激活剂 |
54494ES76/80 |
500 mg/1 g |
|
|
TLR4信号的选择性抑制剂,具有抗炎活性 |
53767ES05/08 |
2/5 mg |
|
|
38MAPK抑制剂,具有抗炎和抗关节炎活性,可缓解疼痛 |
57845ES05/08/10/50 |
2/5/10/50 mg |
|
|
抑制LPS诱导的TNF- alpha释放 |
50810ES08/10 |
5/10 mg |
|
|
抑制NF-κB p65与DNA结合阻止IκB-α磷酸化 |
56084ES08/10/25 |
5/10/25mg |
|
|
抑制LPS刺激的COX-2表达和NF-KB活化 |
55496ES76 |
500 mg |
参考文献
[1]王颖.脂多糖信号通路中的蛋白质修饰[J].中国生物化学与分子生物学报,2008,(06):505-511.DOI:10.13865/j.cnki.cjbmb.2008.06.013.
[2]戴晴.维生素D受体对脓毒症相关急性肾损伤糖代谢重编程的影响研究[D].中南大学,2023.DOI:10.27661/d.cnki.gzhnu.2023.000345.
[3]张震.白藜芦醇调控Nrf2表达及易位在胆色素结石形成中的作用机制研究[D].中国医科大学,2023.DOI:10.27652/d.cnki.gzyku.2023.002120.
[4]林庆州,陈奕颖,宋心茹,等.植物精油对脂多糖攻毒断奶仔猪脾脏损伤的保护作用[J/OL].中国畜牧杂志,1-13[2024-08-15].https://doi.org/10.19556/j.0258-7033.20240104-02.
[5]李尊泰.Nb_2C纳米片层通过αTAT-1下调微管乙酰化水平治疗大鼠牙周炎的机制研究[D].吉林大学,2023.DOI:10.27162/d.cnki.gjlin.2023.007717.





