Q:初始DNA 投入量范围是多少?
A:12201 适用于 500 pg-500 ng Fragment DNA 样本
Q:建库试剂盒里面包含接头吗?
A:建库试剂盒一般都是不包含接头,接头有设置单独的货号,可根据平台和样本数量等选择。
Q:12199ES 和 12201ES的区别是什么?怎么选?
A:扩增模块不同,如果需要高产量扩增,推荐 12199ES建库试剂盒;如后续对保真度要求较高,比如做 SNP 检测相关,则选择12201ES建库试剂盒。
Q:12199 12200 建库一次需要多少磁珠?
A:磁珠用量可参考下表:
| 建库类型 | 需使用磁珠的步骤 | 单个样本需磁珠量 | 96T样本需磁珠量 | 60mL磁珠需配套试剂盒数量 |
| DNA | 常规流程 | 纯化(0.6×),纯化(0.9×) | 105μL | 10.08mL | 6.0个96T建库试剂盒 |
| 纯化(0.6×),纯化(0.9×),分选(0.8/0.2×) | 205μL | 19.68mL | 3.0个96T建库试剂盒 |
| 减半(扩增模块减半) | 纯化(0.6×),纯化(0.9×) | 75μL | 7.2mL | 8.3个96T建库试剂盒 |
| 纯化(0.6×),纯化(0.9×),分选(0.8/0.2×) | 175μL | 16.8mL | 3.6个96T建库试剂盒 |
| 全部体系减半 | 纯化(0.6×),纯化(0.9×) | 52.5μL | 5.04mL | 11.9个96T建库试剂盒 |
| 纯化(0.6×),纯化(0.9×),分选(0.8/0.2×) | 152.5μL | 14.64mL | 4.1个96T建库试剂盒 |
产品操作:
Q:为什么末端修复/加 A 步骤需要开热盖而接头连接不开?
A:末端修复的时候有一步是 72℃,打开热盖防止反应液的冷凝情况,保证反应液体不损失。而接头连接温度较低,影响不大所以关掉热盖。
Q:针对FFPE 样本建库,有没有特殊的建议?
A:针对低质量 FFPE 样本也能取得较好的文库质量,如客户追求更高的文库产量,客户可以选购石蜡样本修复试剂(Cat#12606)。该试剂可以在末端修复时同步进行样本修复,无需额外的实验步骤。
Q:12199ES和 12201ES 建库中都需要哪些酶?
A:1)末端修复/加 A: T4 DNA 聚合酶耐高温 Taq 酶;2)T4 多聚核苷酸激酶(T4 PNK);3)接头连接
T4 DNA 连接酶;4)12201ES 对应的扩增模块式 12621/12624 高保真 DNA 聚合酶;12199 对应的扩增模块是 12620 高扩增效率的。
Q:接头连接之后可以直接进行分选吗?
A:不可以,Ligation Enhancer 内含高浓度的PEG,会对分选造成显著影响,所以接头连接后如果进行
片段分选必须先纯化。
Q:FFPE 样本修复试剂对建库具体的影响是什么?
A:FFPE 样本修复试剂针对石蜡样本的切口,缺刻以及末端氧化的情况可有效进行修复。对文库来说最直观的影响在于产量的提升,而对于测序质量如 Coverage 等无明显作用。而且修复试剂的修复作用,有额外引入突变的可能,肿瘤等客户不建议使用。
结果分析
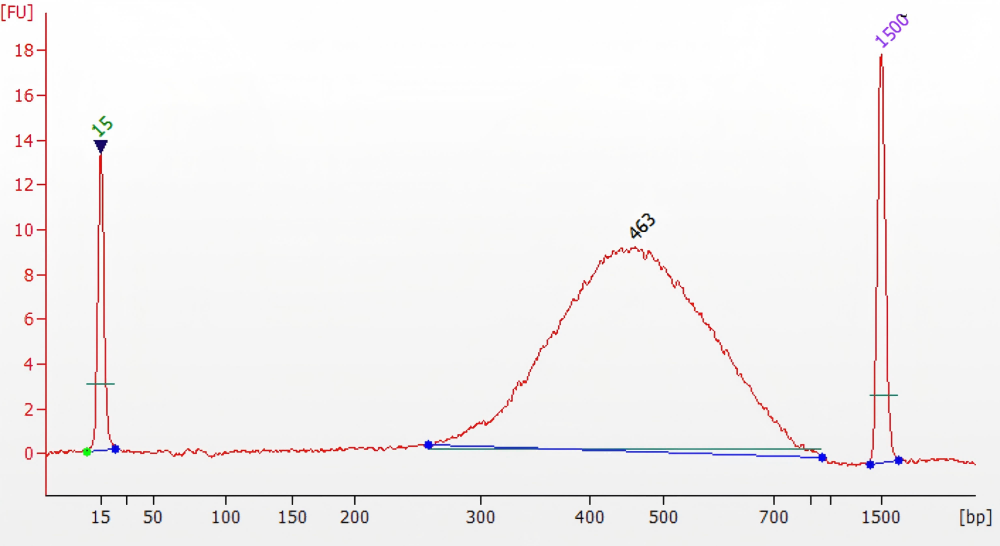
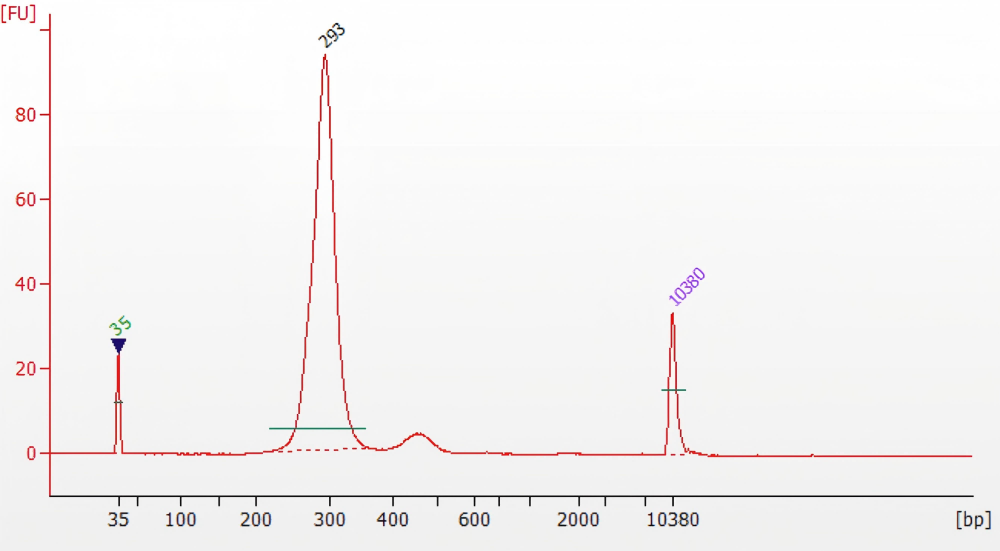
Q:文库片段大小分布一般是什么样的?
A:因为二代测序技术的读长有限,根据不同的测序需求,仪器型号,以及测序模式(单端还是双端测序),一般在 200-800bp 范围内。
Q:不同测序深度Coverage 解读?
A:Coverage 即基因组覆盖度,指的是测序获得的序列占整个基因组的比例。不同测序深度下序列的coverage 肯定也是有差异的。简单来说,10×意思就是说有 10 个测序 reads map 到基因组的某个位置,200×是说有 200 个测序 reads map 到基因组的这个位置。一般情况下测序深度越高,coverage 也会随之降低。
Q:构建得到的文库产量低
A: (1) DNA 质量低,样本中含抑制物(抑制酶活性等)
Input DNA 制备过程中带入的高浓度金属离子螯合剂或者其他盐,可能会影响末端修复以及 A 尾添加等步骤的反应效率,DNA 在TE 溶液中进行片段化,不要在无菌超纯水中进行。
(2)RNA 污染:样本中存在RNA 污染会导致DNA 定量不准确,使文库构建时DNA 上样量不足。
(3)PCR free 的时候上样量不足:当使用完整接头且Input DNA 大于 200 ng 时候,不用 PCR 扩增。如果文库拷贝数过低不能进行直接测序,可在接头连接完成后对DNA 文库进行PCR 扩增。
(4)接头出现降解:接头存储不当会出现降解,影响连接效率。一般稀释过的接头可在室温放置 48h。判断接头是否降解的方法:
a. 用安捷伦 2100 毛细血管电泳检测,通过电泳条带大小判断;如果未发生降解,则条带大小大概为 62bp(complete adapter),如果发生降解,则无条带或条带很小。
b. 用Qubit 酶标仪等检测仪器进行浓度测量,粗略判断接头是否降解。检测方法:取 1uL,15uM 的complete 接头(12615ES-12618ES)若 Qubit 检测浓度 600ng/ul 左右,则接头正常,反之若小于 600ng/ul,则接头可能降解成单链或小片段。酶标仪检测同理。
Q:文库电泳的时候条带异常
A:主要有以下原因造成文库大小异常:
1. 出现小片段(60-120bp):小片段一般为接头片段或接头所形成的二聚体,一般可用 12601 DNA 磁珠进行纯化;
2. 文库富集之后出现大片段:一般文库接头在 120 bp 左右,若文库片段增加幅度超过了 120bp 则可能是扩增过度,导致片段扩增异常。此时需减少PCR 循环数;
3. 接头连接前片段异常,片段化时间或者条件选择不当。