耐高盐全能核酸酶-无惧高盐环境,残留核酸去除更彻底
残留核酸法规监管要求
国家药品监督管理局药品评审中心(CDE)发布的关于基因治疗产品指导原则中明确指出需对DNA残留量和残留片段大小进行控制,建议尽量将DNA残留片段的大小控制在200 bp以下。药典中规定酵母、大肠杆菌表达的生物制品中DNA残留量不超过10 ng/剂量。我国2020年药典将人用狂犬病疫苗(Vero细胞)DNA残留标准更新为≤3 ng/剂量。
为了确保生物制品中的核酸残留符合相应法规要求,在生物制品的生产工艺中包含去除核酸残留的关键步骤显得至关重要。
残留核酸去除面临的挑战
随着生产工艺复杂性不断升高,在高盐环境下有效去除残留核酸面临众多新的挑战:
AAV病毒纯化过程中,为了提高病毒回收率,通常会使用更高盐浓度的buffer(200-500 mM),但是常规全能核酸酶会随着盐浓度升高,活性显著下降,如果通过加大酶用量及孵育时间来提高纯化效果,会大大增加成本;
宿主DNA通常以染色质形式存在,容易被蛋白包裹,导致DNA无法暴露,而在高盐环境下,核酸和蛋白质能够有效分离,从而更好的去除残留核酸;
为满足在高盐环境下能够提高AAV病毒纯化回收率及高效去除残留核酸,翌圣生物依托酶改造平台,自主开发出耐高盐全能核酸酶,在500 mM高盐环境中仍有高酶活,有效解决高盐环境去除残留核酸困难的问题。
残留核酸去除利器-耐高盐全能核酸酶
Salt Active UltraNuclease GMP-grade(耐高盐全能核酸酶)是一种来源于海洋微生物的重组非特异性核酸内切酶,与UltraNuclease相比在500 mM Na+条件下具有最佳活性,在高盐环境中,有效去除核酸污染。本品经基因工程改造在Escherichia coli (E. coli)中表达纯化,应用在病毒纯化、疫苗生产、蛋白和多糖类制药工业作为宿主残留核酸去除试剂,能够有效去除宿主残留核酸,保证生物制品功效及安全性。
产品满足审计需求,目前已助力多家企业顺利完成IND申报,项目经验丰富。
产品优势
-
无惧高盐环境:500 mM 盐浓度条件下酶活最高
-
提高病毒收率:高盐环境减少AAV颗粒聚集,提高病毒回收率
-
产品质量可靠:GMP级别产品;无动物源、无抗生素;
-
完成DMF备案:备案号MF037815
耐高盐全能核酸酶产品性能测试
高盐环境对酶活的影响(Na+)
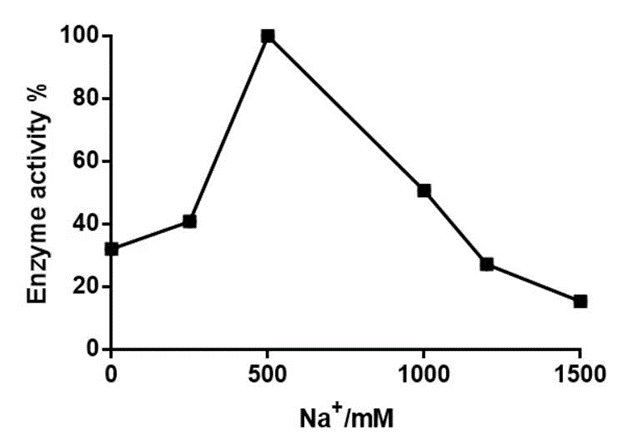
耐高盐全能核酸酶在Na+浓度为500 mM时酶活最佳,较常规全能核酸酶而言,在高盐环境下更有优势。
更多检测指标可发送邮件获取,邮箱地址:
-
marketing@yeasen.com
耐高盐全能核酸酶推荐反应条件
|
条件参数 |
最佳条件 |
有效条件 |
|
Mg2+ |
20 mM(10-50 mM) |
1~100 mM |
|
PH |
8 |
6.5 ~10 |
|
温度 |
37℃ |
4~42℃ |
|
Na+/K+ |
500 mM |
300~1000 mM |
应用案例
核酸消化能力-案例1
案例描述:相同质粒样本经不同厂家酶处理,通过琼脂糖凝胶电泳检测质粒消化效果

1、 阴性对照 ,2、竞品S ,3、竞品H ,4、Yeasen ,5、竞品K
结果:Yeasen 产品在4个品牌平行测试中,酶切效果最好。
核酸消化能力-案例2
案例描述:病毒生产中,高盐环境下(400 mM)经Yeasen和竞品A同时进行消化,通过qPCR检测293宿主残留核酸。
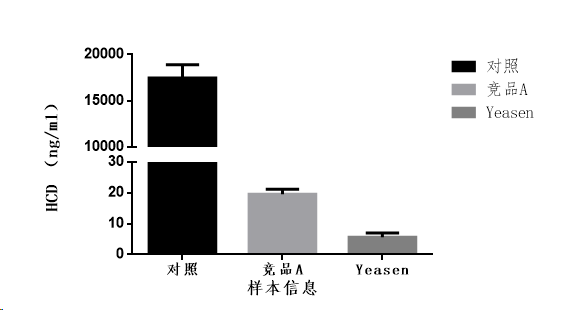
结果:Yeasen 耐高盐全能核酸酶性能优于国外耐高盐竞品;
为了匹配耐高盐全能核酸酶的使用,翌圣生物也自主研发了能够特异性检测耐高盐全能核酸酶检测试剂盒,能够有效检测出酶的残留,降低风险。翌圣耐高盐全能核酸酶残留检测试剂盒验证方法参考2020中国药典<9101>分析方法验证指导原则进行研发生产,严格按照要点要求进行多指标检测(线性范围、专属性、准确度、精密度、灵敏度、加速稳定性等)。
耐高盐全能核酸酶残留检测试剂盒
耐高盐全能核酸酶残留检测试剂盒可特异性检测耐高盐全能核酸酶,试剂盒检测灵敏度为0.047 ng/mL,线性检测范围是0.047-3 ng/mL。
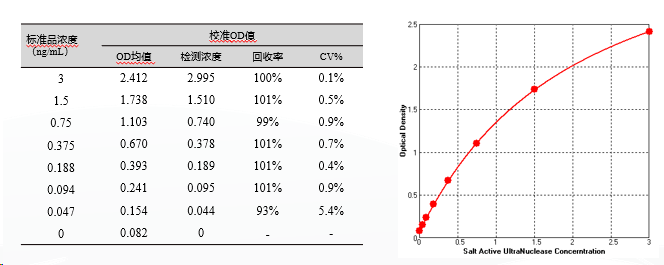
翌圣生物始终以高标准和高质量要求自己,目前已建立了完善的质量体系,确保产品一致性、可靠性,并满足中外项目申报的需求。
质量体系
翌圣生物致力于提供高质量产品,具有较好的批间一致性,产品质量稳定可靠;所有产品研发、生产都符合ISO13485质量管理体系,按照GMP要求生产;产品原辅料均严格把控,符合GMP生产标准,能够满足客户文件审计及现场审计需求;武汉GMP生产基地配备工业级AKTA纯化与理化分析设备、百升级高密度发酵机组、万级标准洁净车间、自动化生产线,基地占地3000平,单次发酵可达800 L。

订购产品信息
|
产品名称 |
产品货号 |
产品规格 |
|
Salt Active UltraNuclease GMP-grade 耐高盐全能核酸酶 |
20159ES25/50/60/80/90 |
25KU/50KU/100KU/1MU/5MU |
|
Salt Active UltraNuclease ELISA kit耐高盐全能核酸酶检测试剂盒 |
36703ES96 |
96T |
其他相关产品信息
|
产品名称 |
产品货号 |
产品规格 |
|
UCF.ME®UltraNuclease GMP-grade全能核酸酶(同Benzonase) |
20157ES25/50/60/80/90 |
25KU/50KU/100KU/1MU/5MU |
|
UCF.ME® UltraNuclease ELISA Kit全能核酸酶检测试剂盒 |
36701ES59 |
96T |
