干货│从原理到应用,带你全方面了解T4 gene 32 protein
T4噬菌体基因32编码蛋白(T4 gene 32 protein,gp32)是一种单链DNA(ssDNA)结合蛋白,为T4噬菌体DNA复制和修复所必需。它被广泛地用于稳定和标记ssDNA区域,以便用电子显微镜观察细胞内DNA的结构、促进限制性内切酶的消化反应、提高RT-PCR中反转录的效率、增强T4 DNA聚合酶的活性和提高PCR的产量等。
-
核心结构域:包含ssDNA的结合位点,并具区分单链、双链DNA的能力;
-
C端结构域(CTD):涉及异型蛋白相互作用,带负电荷,调节gp32与复制、修复和重组机制中其他成分的相互作用;
-
N端结构域(NTD):负责同型蛋白相互作用,带正电荷,与邻近的gp32单体的核心结构域之间通过蛋白-蛋白接触,使gp32蛋白以头-尾方向结合ssDNA。
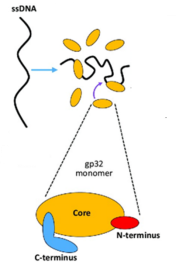
图1. gp32结构域[1]
当前导链聚合酶(红色)在DNA损伤处(X)停滞时,前导链和后随链的合成会解耦联,后随链的合成机制可以合成与受损部位重叠的冈崎片段(绿线),同时会在停滞的前导链聚合酶前面打开一个ssDNA缺口,该缺口被gp32覆盖(橙色);
模板子链3 '端解旋
gp32单体簇通过阻止Dda解旋酶加载到后随链上来阻止其对复制叉移动的刺激,并促进模板子链3 '端的解旋;
模板转换恢复复制叉移动
UvsX重组酶和Dda解旋酶催化模板转换来恢复停滞的复制叉;
跨损伤DNA合成
进行后续无错误的跨损伤DNA合成。
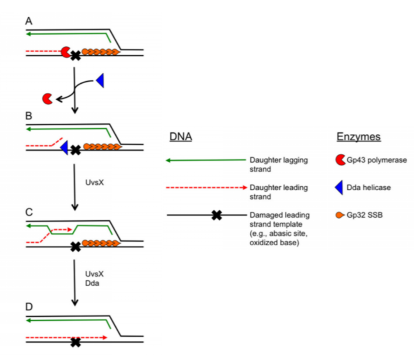
图2. gp32介导的重组修复过程[2]
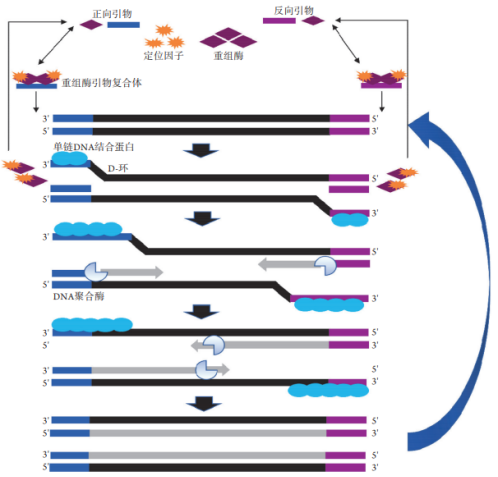
图3. 重组酶聚合酶扩增RPA技术扩增原理图[3]
RPA具体流程如下:
重组酶T4 UvsX在ATP的参与和定位因子(T4 UvsY)的帮助下与扩增引物结合形成重组酶引物复合体,并在双链DNA中寻找同源序列;
重组酶引物复合体一旦定位到同源序列,则会插入双链DNA形成D-环结构,启动链置换反应,单链结合蛋白gp32会与解开的DNA链结合防止进一步被置换;
重组酶T4 UvsX从重组酶引物复合体中被水解,3'端引物暴露并与Bsu DNA聚合酶结合,DNA开始复制延伸,最终两条母链分离,形成两条新的互补双链DNA。该反应在37-42℃下进行,可在30 min内实现目标序列1012倍的扩增。
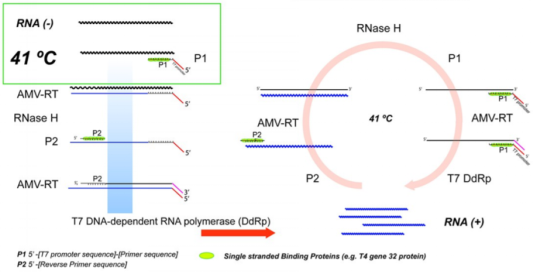
图4. NASBA工作流程图[4]
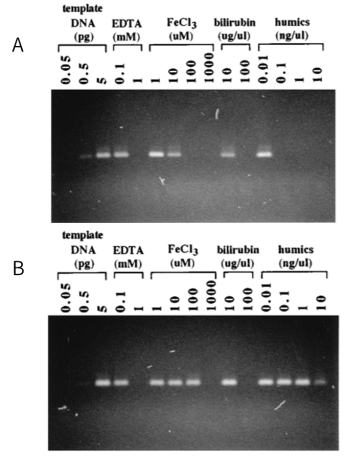
图5. T4 gene 32 protein解除抑制剂对PCR的干扰[6]。A:不含gp32的标准PCR条件;B:含有150 ng/mL gp32的PCR条件
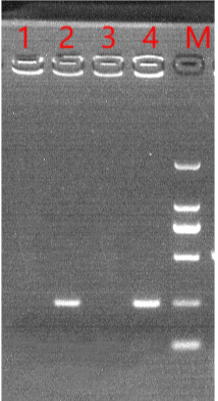
图5.客户测试翌圣重组酶聚合酶核心酶原料扩增结果图
注:2、4为阳性实验组;1、3为阴性对照组
|
产品名称 |
产品货号 |
产品作用 |
|
Bsu DNA polymerase (Large fragment, 5 U/μL) |
结合引物与原始靶核酸序列互补合成新的DNA模板 |
|
|
T4 UvsX Recombinase (2 μg/μL) |
具有配对和链转移活性的重组酶 |
|
|
T4 UvsY protein (2 μg/μL) |
重组酶辅助因子,刺激T4 UvsX的单链DNA依赖性ATP酶活性并降低活性所需的T4 UvsX临界浓度 |
|
|
T4 gene 32 protein (gp 32) T4噬菌体基因32编码蛋白 |
参与DNA复制、修复、重组与解链后的单链DNA结合,防止自杂交 |
|
|
Creatine Kinase (2 μg/μL) 肌酸激酶 |
刺激ATP和肌酸分解为磷酸肌酸和ADP,释放能量 |
|
|
Exonuclease III (100 U/μL) |
具有3’→5’外切酶活性,切断荧光探针中淬灭基团,释放荧光 |
