涨知识|qPCR专场四:问题图表分析及实验案例
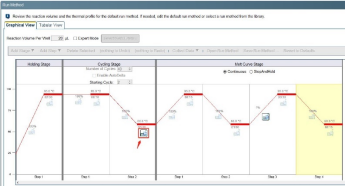
仪器界面展示处以7500为例
-
引物冻干粉在长时间储存和储存温度上有着更强的灵活性和保障;
-
引物浓度对稳定性也会产生影响,不建议以低于10μM的浓度储存引物,在大多数情况下,100μM的引物使用更加灵活容易;
-
引物或探针也需和RNA一样分装储存,以尽可能减少反复冻融带来的影响;
-
TE缓冲液的储存环境比水更加稳定。
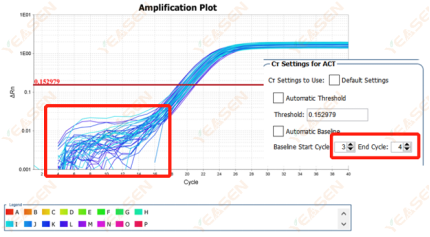
原因分析及解决方案:
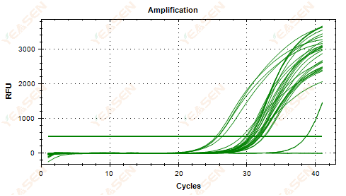
在对数图扩增曲线中,若基线期为连续曲线,则有可能是基线期设置循环周期偏少造成。可以在设置中增大基线的终点值,调整后可恢复正常,如下图所示:

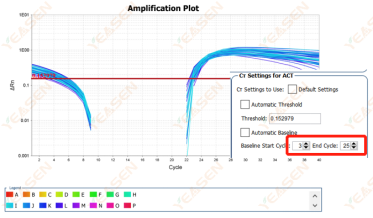
原因分析及解决方案:
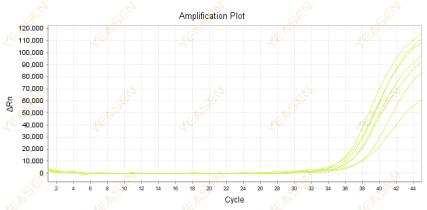
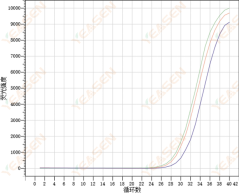
在对数图扩增曲线中,若扩增曲线基线期连续且后续出现明显分段现象,则有可能是基线期设置循环周期偏多造成。可以在设置中减小基线的终点值,调整后可恢复正常,如下图所示:

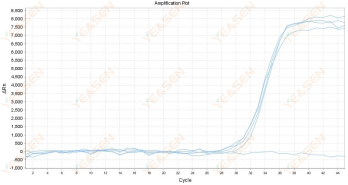


原因分析及解决方案:
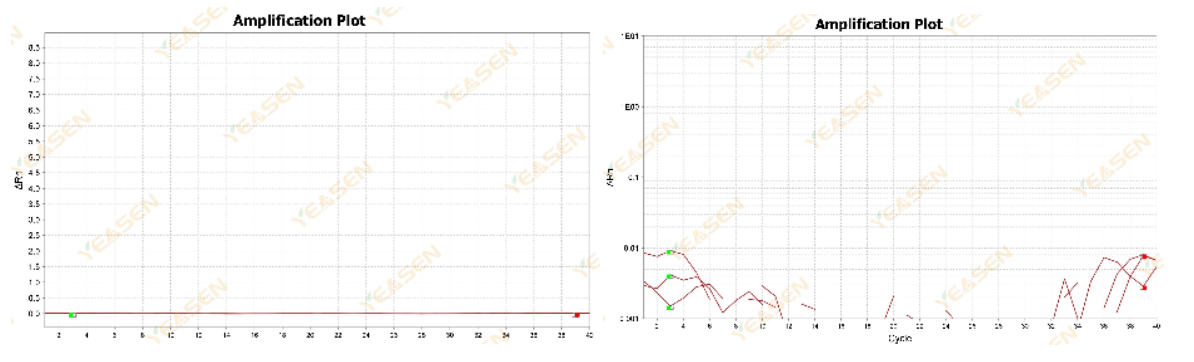
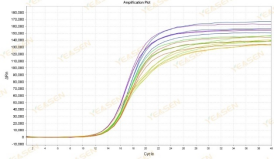
可能是ROX浓度与机型不能匹配造成这种现象。建议在设置中找到Passive Reference后将ROX改为None,重新分析即可获取正常的扩增曲线,如下图所示。
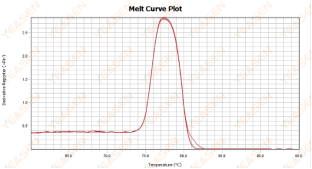
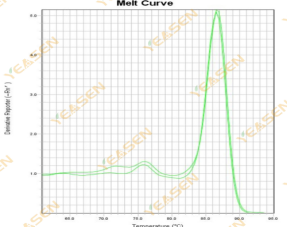
-
优化热循环条件,主要是提高退火温度;
-
降低引物浓度。在多数情况下,引物终浓度为200 nM,可选择降低至60 nM;
-
第一次针对一个靶标设计引物时,可尝试设计三对引物组,选用其中效率最高、特异性表现最好的引物进行实验。
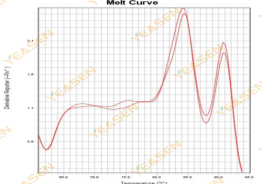
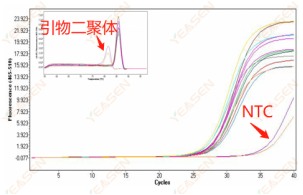
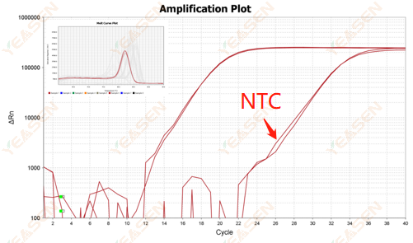
引物二聚体导致的非特异扩增,具体解决方案可见上述【熔解曲线为双峰且较低峰Tm在80℃之前】。其中值得注意的点是,若实验组和阴性对照组之间的Ct值差值远大于10,则表示引物二聚体对于靶标片段扩增的影响不大,数据可用于分析。
|
方法 |
分类 |
产品名称 |
货号 |
|
RNA提取 |
同Trizol提取 |
TRIeasy™ Total RNA Extraction Reagent |
|
|
动物组织/细胞总RNA提取,避开有毒试剂,最快15 min完成 |
MolPure® Cell/Tissue Total RNA Kit细胞/组织总RNA提取试剂盒 |
||
|
简单植物总RNA提取,避开有毒试剂,最快40min完成 |
MolPure® Plant RNA Kit 植物RNA提取试剂盒 |
||
|
多糖多酚植物总RNA提取,最快30min完成 |
MolPure® Plant Plus RNA Kit 多糖多酚植物RNA提取试剂盒 |
||
|
细胞总RNA提取,避开有毒试剂,最快8 min完成 |
MolPure® Cell RNA Kit 培养细胞RNA提取试剂盒 |
||
|
qPCR染料法 |
高灵敏通用型定量预混液(染料法) |
Hieff UNICON® Universal Blue qPCR SYBR Master Mix |
|
|
超高性价比定量预混液 (染料法),已发文章累计IF达到5000+ |
Hieff® qPCR SYBR Green Master Mix (No Rox) |
||
|
Hieff® qPCR SYBR Green Master Mix (Low Rox) |
|||
|
Hieff® qPCR SYBR Green Master Mix (High Rox) |
|||
|
高灵敏型qPCR预混液(染料法) |
Hieff UNICON® qPCR SYBR Green Master Mix (No Rox) |
||
|
Hieff UNICON® qPCR SYBR Green Master Mix (Low Rox) |
|||
|
Hieff UNICON® qPCR SYBR Green Master Mix (High Rox) |
|||
|
miRNA加A法高特异性定量预混液(染料法) |
Hieff® miRNA Universal qPCR SYBR Master Mix(加A法) |
||
|
miRNA茎环法高特异性定量预混液(染料法) |
Hieff® miRNA Universal qPCR SYBR Master Mix(茎环法) |
||
|
高灵敏一步法反转定量试剂盒(染料法) |
Hifair® III One Step RT-qPCR SYBR Green Kit |
||
|
细胞直扩RT-qPCR,1.5 h从细胞到基因表达分析(染料法) |
Hieff® Fast Cell Direct SYBR Green RT-qPCR Kit |
||
|
反转录试剂 |
5 min快速反转,最长可满足14 kb cDNA合成,含gDNA去除(下游应用PCR/qPCR)-示踪版New |
Hifair® AdvanceFast 1st Strand cDNA Synthesis Kit |
|
|
5 min快速反转,最长可满足14 kb cDNA合成,含gDNA去除(下游应用PCR/qPCR)-常规版New |
Hifair® AdvanceFast 1st Strand cDNA Synthesis Kit(No Dye) |
||
|
15 min一步完成gDNA去除与反转录(下游应用qPCR) |
Hifair® V one-step RT-gDNA digestion SuperMix for qPCR |
||
|
高质量第一链cDNA合成预混液,含gDNA去除(下游应用qPCR) |
Hifair® III 1st Strand cDNA Synthesis SuperMix for qPCR (gDNA digester plus) |
||
|
最长可满足19.8 kb cDNA合成试剂盒,含gDNA去除(下游应用PCR/qPCR) |
Hifair® III 1st Strand cDNA Synthesis Kit(gDNA digester plus) |
||
|
常规30 min反转预混液,含gDNA去除(下游应用qPCR) |
Hifair® II 1st Strand cDNA Synthesis SuperMix for qPCR (gDNA digester plus) |
||
|
miRNA反转录试剂盒(加A法) |
Hifair® miRNA 1st Strand cDNA Synthesis Kit (加A法) |
