PEI转染试剂-病毒载体生产上游工艺的核心物料
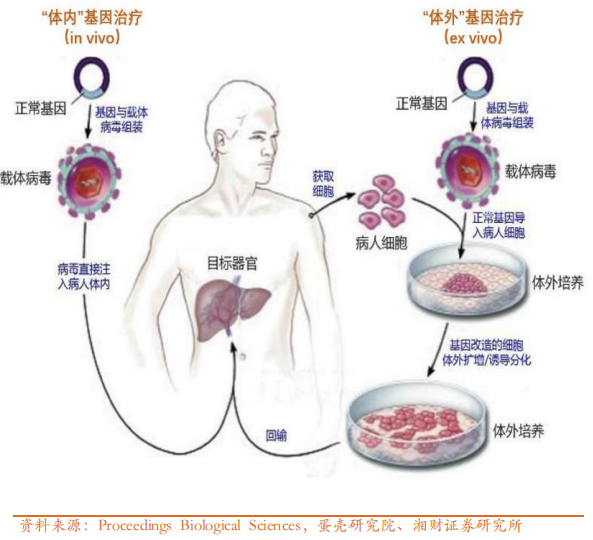
病毒载体
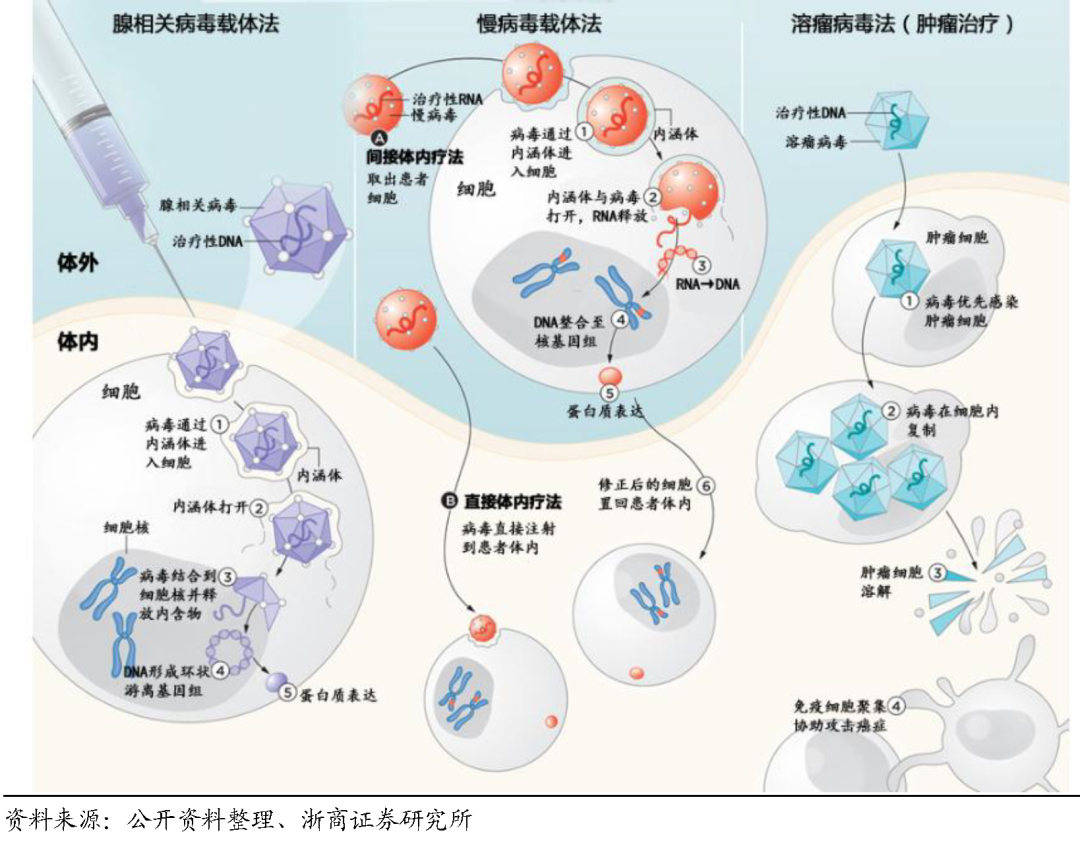
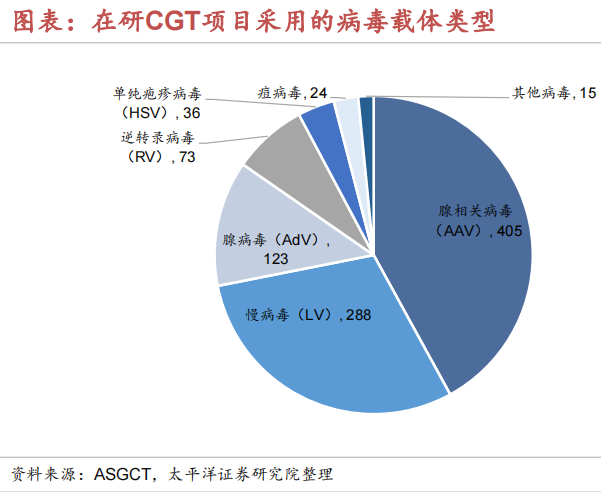
病毒载体的生产
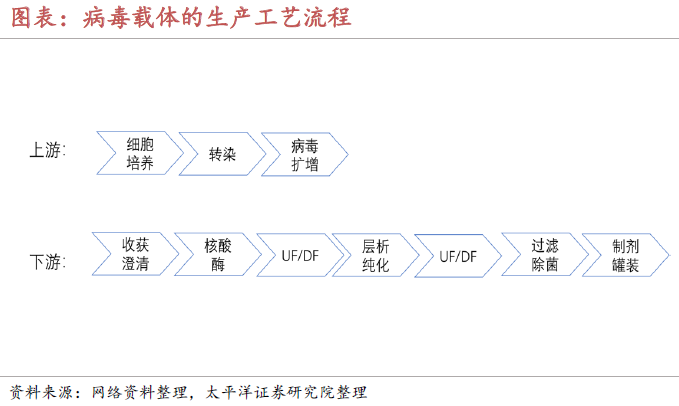
转染试剂
产品特点
产品信息
|
产品名称 |
货号 |
规格 |
|
40820 |
1.5 mL/10 mL/100 mL |
|
|
40821 |
1 L/10 ml/100 ml |

病毒载体


病毒载体的生产


转染试剂
产品特点
产品信息
|
产品名称 |
货号 |
规格 |
|
40820 |
1.5 mL/10 mL/100 mL |
|
|
40821 |
1 L/10 ml/100 ml |